Sifat Kimia, Fungsi, Fermentasi, Reaksi Kimia, Pembuatan Asam Asetat
Asam asetat (CH3COOH) juga disebut asam etanoat, asam karboksilat yang paling penting. Larutan asam asetat encer (sekitar 5 persen volume) yang dihasilkan melalui fermentasi dan oksidasi karbohidrat alami disebut cuka; garam, ester atau asil asam asetat disebut asetat.
Dalam industri, asam asetat digunakan dalam pembuatan asetat logam, yang digunakan dalam beberapa proses pencetakan. Vinil asetat, digunakan dalam produksi plastik. Selulosa asetat, digunakan dalam film fotografi dan tekstil. Dan ester organik yang mudah menguap (seperti etil dan butil asetat), banyak digunakan sebagai pelarut untuk resin, cat, dan lak. Secara biologis, asam asetat adalah perantara metabolisme yang penting, dan asam asetat terjadi secara alami dalam cairan tubuh dan dalam jus tanaman.
Sifat kimia Asam asetat
Keasaman
Atom hidrogen (H) dalam gugus karboksil (−COOH) dalam asam karboksilat seperti asam asetat dapat dilepaskan sebagai ion H + (proton), memberi mereka sifat asam. Asam asetat adalah asam monoprotik yang lemah dan efektif dalam larutan air, dengan nilai pKa 4,8. Basis konjugat adalah asetat (CH3COO−). Larutan 1,0 M (tentang konsentrasi cuka domestik) memiliki pH 2,4, menunjukkan bahwa hanya 0,4 persen molekul asam asetat yang dipisahkan.
Dimer siklik
Struktur kristal asam asetat menunjukkan bahwa molekul berpasangan menjadi dimer yang dihubungkan oleh ikatan hidrogen. Dimer juga dapat dideteksi dalam uap pada 120 ° C. Mereka juga terjadi dalam fase cair dalam larutan berair dalam pelarut non-ikatan hidrogen, dan sampai batas tertentu dalam asam asetat murni, tetapi terganggu oleh pelarut ikatan hidrogen. Entalpi dimer disosiasi diperkirakan 65,0-66,0 kJ / mol, dan entropi disosiasi pada 154-157 J mol – 1 K – 1. Perilaku dimerisasi ini dimiliki oleh asam karboksilat rendah lainnya.
Pelarut
Asam asetat cair adalah pelarut protik hidrofilik (polar), mirip dengan etanol dan air. Dengan konstanta dielektrik moderat 6,2, ia dapat melarutkan tidak hanya senyawa polar seperti garam dan gula anorganik, tetapi juga senyawa non-polar seperti minyak dan unsur-unsur seperti belerang dan yodium. Ini mudah dicampur dengan banyak pelarut polar dan non-polar lainnya seperti air, kloroform, dan heksana. Larutan dan ketidakmampuan asam asetat membuatnya menjadi bahan kimia industri yang banyak digunakan.
Reaksi kimia asam asetat
Asam asetat bersifat korosif terhadap banyak logam termasuk besi, magnesium dan seng, membentuk gas hidrogen dan garam logam yang disebut asetat. Aluminium, ketika terkena oksigen, membentuk lapisan tipis aluminium oksida pada permukaannya yang relatif tahan, sehingga tangki aluminium dapat digunakan untuk mengangkut asam asetat. Logam asetat juga dapat dibuat dari asam asetat dan basa yang sesuai, seperti dalam reaksi “baking soda + cuka” yang populer. Dengan pengecualian kromium (II) asetat, hampir semua asetat larut dalam air.
Asam asetat mengalami reaksi kimia khas dari asam karboksilat, seperti memproduksi asam etanoat ketika bereaksi dengan alkali, menghasilkan logam etanoat ketika bereaksi dengan logam, dan menghasilkan logam etanoat, air dan karbon dioksida ketika bereaksi dengan karbonat dan hidrogen karbonat.
Yang paling menonjol dari semua reaksi adalah pembentukan etanol oleh reduksi, dan pembentukan turunan seperti asetil klorida dengan apa yang disebut “substitusi asil nukleofilik.” Turunan substitusi lain termasuk anhidrida asetat; Anhidrida ini dihasilkan oleh hilangnya air dari dua molekul asam asetat.
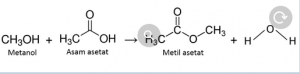
Ester asam asetat juga dapat dibentuk melalui esterifikasi Fischer, dan amida juga dapat dibentuk. Ketika dipanaskan di atas 440 ° C, asam asetat terurai untuk menghasilkan karbon dioksida dan metana, atau keten dan air.
Deteksi asam asetat
Asam asetat dapat dideteksi oleh baunya yang khas. Reaksi warna untuk garam asam asetat adalah larutan besi (III) klorida, yang menghasilkan warna sangat merah yang hilang setelah pengasaman. Asetat ketika dipanaskan dengan arsenik trioksida membentuk cacodyl oxide, yang dapat dideteksi dengan uap berbau busuk.
Rumus kimia asam asetat
Cuka memiliki formula empiris C2H4O2. Formula ini sering ditulis dalam bentuk CH3 – COOH, CH3COOH, atau CH3CO2H. Asam asetat pekat (disebut asam asetat glasial) adalah cairan higroskopis yang tidak berwarna, dan memiliki titik beku 16,7 ° C.
Pembuatan asam asetat
Pembentukan asam asetat melibatkan 2 perubahan kimia, yaitu fermentasi alkohol dari karbohidrat, dan oksidasi alkohol menjadi asam asetat.
Perbedaan asam cuka yang dihasilkan tergantung pada substrat yang digunakan. Untuk produksi fermentasi ragi asam asetat digunakan. Konsentrasi alkohol diatur sehingga mencapai sekitar 10-13%, kemudian bakteri yang membentuk asam asetat ditambahkan
Peralatan yang digunakan dimaksudkan agar bakteri dapat melakukan proses oksidasi menjadi alkohol. Salah satu metode, metode Frigs, dijelaskan sebagai berikut: Campuran yang terdiri dari cairan tertentu terkonsentrasi dengan asam asetat asam dan nutrisi tertentu yang dibutuhkan oleh pertumbuhan bakteri pembentuk asam asetat.
Bakteri dalam genus Acetobacter dimasukkan ke dalam campuran “serutan kayu beeachwood” yang dimasukkan melalui bak di bagian atas alat. Ketika alkohol melewati gergaji ini, bakteri mengubah sebagian alkohol menjadi asam asetat. Campuran yang dikumpulkan di bagian bawah dituangkan kembali ke kayu gergajian, menghasilkan lebih banyak asam asetat. Proses ini merupakan proses aerobik sehingga dibutuhkan oksigen untuk pembentukan asam asetat.
Fungsi dan Kegunaan asam asetat
- Asam asetat digunakan sebagai bahan baku untuk membuat selulosa asetat, yang umum digunakan dalam industri film.
- Sebagai bahan baku pembuatan polyvinyl acetate, yang merupakan bahan baku pembuatan lem kayu.
- Digunakan sebagai pelarut dalam proses produksi industri.
- Digunakan untuk membuat tinta dan pewarna.
- Di laboratorium klinis, digunakan sebagai bahan untuk pengujian darah.
- Digunakan dalam industri pembotolan minuman ringan.
- Digunakan dalam industri manufaktur karet dan plastik.
- Asam asetat juga digunakan dalam proses pembuatan pestisida.
- Dalam industri makanan, asam asetat telah disetujui sebagai aditif makanan dengan nomor registrasi E260.
- Di Indonesia, asam asetat sering digunakan sebagai bahan untuk mengawetkan makanan, seperti membuat manisan buah atau sayuran.
- Di sektor kesehatan, konsentrasi asam asetat yang rendah biasanya digunakan sebagai deodoran anti bakteri dan alami, yaitu zat penghilang bau.
- Asam asetat memainkan peran penting sebagai zat yang digunakan untuk membersihkan noda pada kaca, benda yang terbuat dari kuningan, baja dan kerak pada pembuat kopi.
- Selain itu, asam asetat juga bisa digunakan untuk menghilangkan bau kencing di toilet dan kamar mandi.
Fermentasi Asam Asetat
Assifikasi adalah proses oksidasi etanol oleh bakteri menjadi asam asetat dan air. Kelompok bakteri yang mengoksidasi etanol menjadi asam asetat disebut bakteri asam asetat. Bakteri yang biasa digunakan adalah Acetobacter aceti. Secara kimia proses oksidasi adalah:
C2H5 OH + O2 → CH3 COOH + H2 O
Etanol Oksigen Asam Asetat Air
Etanol oksigen Sebagai. Setara Air 132 Cuka asam tidak boleh bersentuhan dengan udara, karena dapat dioksidasi lebih lanjut menjadi air dan karbon dioksida. Karena itu asam cuka harus ditutup rapat. Reaksi menjadi:
CH3 COOH + 2O2 → 2H2 O + 2CO2