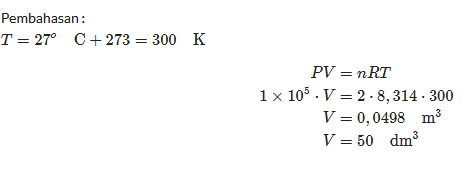Hai teman-teman, semoga selalu dalam keadaan sehat dan sukses ya, admin akan memberikan contoh soal essay dan jawaban serta pembahasan teori kinetik gas ideal. Semoga contoh soal essay dan jawaban serta pembahasan teori kinetik gas ideal tersebut bermanfaat banyak.
Soal No. 1). 16 gram gas Oksigen (M = 32 gr/mol) berada pada tekanan 1 atm dan suhu 27oC. Tentukan volume gas jika:
a) diberikan nilai R = 8,314 J/mol.K
b) diberikan nilai R = 8314 J/kmol.K
Jawaban:
Pembahasan
a) untuk nilai R = 8,314 J/mol.K
Data :
R = 8,314 J/mol.K
T = 27oC = 300 K
n = 16 gr : 32 gr/mol = 0,5 mol
P = 1 atm = 105 N/m2
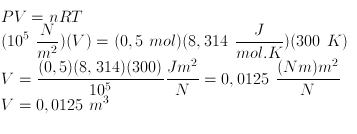
Data :
R = 8314 J/kmol.K
T = 27oC = 300 K
n = 16 gr : 32 gr/mol = 0,5 mol
P = 1 atm = 105 N/m2
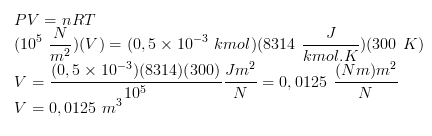
Soal No.2). Suatu gas ideal sebanyak 4 liter memiliki tekanan 1,5 atmosfer dan suhu27oC. Tentukan tekanan gas tersebut jika suhunya 47oC dan volumenya 3,2 liter!
Dik: Kondisi 1
V = 4 L
P = 1,5 atm
T = 27+273=300K
Kondisi 2
V = 3,2 L
T = 47+273=320K
Dit: P2
Jawaban:
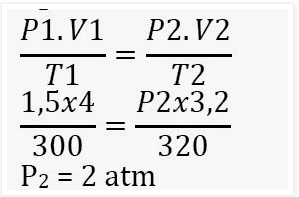
Soal No. 3). Gas oksigen (Mr = 32) massa 80 gram berada dalam tangki yang volumenya 8 liter. Hitunglah tekanan yang dilakukan oleh gas jika suhunya 27 oC ?
Dik: Mr O2 = 32
m = 80 gram
V = 8 liter
T = 300K
R = 8,31 J/mol.K = 0,082 L.atm/mol.K
Dit: P
Jawaban:

Soal No. 4). Pada kondisi awal partikel gas yang berada dalam ruang tertutup memiliki tekanan P, volume V, dan suhu T. Jika gas volumenya diubah menjadi 3/4 V dan suhu diubah menjadi 2T maka perbandingan tekanan awal dengan tekanan setelah V dan T diubah adalah ….
Jawaban:
Data yang diketahui pada soal:
P1 = P
V1 = V
T1 = T
V2 = 3/4 V
T2 = 2T
Berdasarkan persamaan umum gas ideal:
PV = nRT
diperoleh perbandingan:
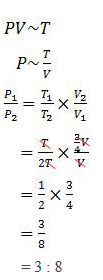
Jadi, perbandingan antara tekanan awal dengan tekanan setelah V dan T diubah adalah 3 : 8
Soal No. 5). Dua mol gas N2 pada suhu 27oC memiliki tekanan 1 atm. Volume gas tersebut adalah ….